3 доступных сильных основания
Определение основания
Основания представляют собой класс соединений, состоящих из положительно и отрицательно заряженных ионов. В качестве положительно заряженного иона – катиона – выступают ионы металлов, анионом чаще всего выступает гидроксид-ион OH-. При диссоциации основание высвобождает гидроксид-ионы, которые могут образовывать связь с водородом. В узком смысле вещества данного класса являются акцепторами протонов. Реакцию основания с кислотой называют реакцией нейтрализации. В ходе превращения кислота отдает водороды на образование связи с гидроксидной группой, которая их принимает, таким образом образуется водный раствор соли.
Показатель кислотности оснований приходится на диапазон от 8 до 14, причем раствор с pH=14 считается сильнейшим основанием. Большинство оснований бесцветные и маслянистые, не имеют запаха, так как нелетучи в отличие от кислот.
Основание и щелочь
Частный случай оснований – щелочи. Данные соединения представляют собой основания щелочных металлов – натрий, калий, литий и т.д. В эту группу соединений также относят основания некоторых других металлов, например, барий, таллий. Щелочи полностью диссоциируют в водном растворе и сами по себе химически активные соединения. Концентрированные щелочи агрессивны, при попадании на кожу и слизистые оболочки вызывают ожоги разной степени тяжести.
Кислоты и основания являются противоположными по взаимодействию с другими веществами. При этом важно отметить, что существуют основания, которые могут выступать, как кислоты, и кислоты, которые могут выступать, как основания. Так как химические взаимодействия очень часто неоднозначны, одни классы соединений могут проявлять нетипичные свойства при определенных условиях. Примером основания, которое проявляет и кислотные свойства, является гидроксид алюминия, который при сплавлении с щелочами образует алюминаты – NaAlO2.
Сильные основания
Как и кислоты, основания могут быть как сильными, так и слабыми. Сильными считаются основания с показателем кислотности от 12 до 14. Чем меньше pH, тем слабее основные свойства и сильнее кислотные. Амфотерные соединения имеют показатель кислотности около 8. Одним из главных свойств сильных оснований является практически полная диссоциация на ионы. Важно отметить, что наряду с суперкислотами существуют также супероснования. Данные вещества являются чрезвычайно сильными представителями своих классов. Далее приведем примеры наиболее сильных оснований, доступных на сегодняшний момент.
Гидроксид лития
Вещество является одновременно сильным основанием и слабой щелочью. В обезвоженном состоянии представляет собой белый кристаллический порошок, полностью растворимый в воде. Гидроксид лития получают обменной реакцией между карбонатом лития и гидроксидом кальция по уравнению реакции:
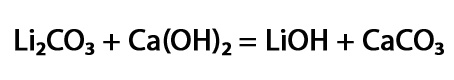
Вещество широко применяется в промышленности. Три главных применения гидроксида лития:
- в качестве компонента при изготовлении мыла, такое мыло называется литиевым;
- в качестве вещества, хорошо абсорбирующего углекислый газ в вентиляции космических ракет, подводных лодок, а также в помещениях, которые необходимо очищать от углекислого газа;
- в качестве компонента при изготовлении литиевых батареек;
- в качестве средства для очистки ржавчины с поверхности металлов.
В нашей компании ООО "Полихим" можно купить гидроксид лития и другие соединения лития по доступной цене. Реактив соответствует стандартам качества.
Гидроксид натрия
Вещество представляет собой сильное основание и сильную щелочь, так как натрий более активный щелочной металл. Как щелочь гидроксид натрия гораздо более агрессивен, чем гидроксид лития. При нормальных условиях концентрированный раствор активно разлагает белки, что делает вещество более опасным для человеческого организма, чем кислоты. В безводном состоянии гидроксид натрия представляет собой белый кристаллический порошок, хорошо растворимый в воде.
В настоящее время считается самым распространенным сильным основанием, производимым в больших количествах. Такая популярность гидроксида обусловлена повышенной химической активностью и полезными свойствами. Можно выделить самые распространенные способы применения вещества:
- в качестве сильного абсорбента углекислого газа и воды из воздуха;
- в качестве компонента на производстве моющих средств;
- на бумажном производстве;
- в производстве строительных смесей и цемента;
- в качестве реактива для нейтрализации кислоты.
Купить гидроксид натрия можно на сайте нашей компании ООО "Полихим" по доступной цене. Реактив соответствует заявленным стандартам качества.
Гидроксид калия
Является сильным основанием и сильной щелочью. Гидроксид калия в обезвоженном состоянии представляет собой белый кристаллический порошок, хорошо растворимый в воде. В растворенном виде бесцветный и не имеет запаха. Гидроксиды натрия и калия примерно равны по химической активности и взаимозаменяемы. Однако наиболее часто используется едкий натр, так как его производство экономически выгоднее.
Гидроксид чрезвычайно активен, благодаря чему легко разрушает поверхности металлов, обугливает древесину и разрушает белки. Концентрированные растворы глубоко проникают в кожу и вызывают сильные долго незаживающие ожоги.
Гидроксид калия способен заменять гидроксид натрия на производствах, поэтому способы применения схожи. Из основных можно выделить:
- производство мыла и моющих средств;
- использование в качестве электролита в производстве аккумуляторов;
- производство биологоческого топлива;
- абсорбция газов и воды.
Купить гидроксид калия можно на сайте нашей компании ООО "Полихим". Реактив чистый, приготовлен в соответствии с установленными стандартами качества.
К другим статьям


